Hvordan virker sigdcelleanemi påvirke Malaria infeksjoner?
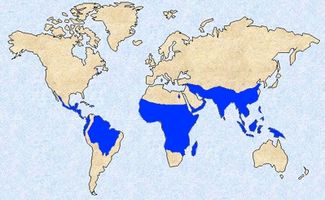
Malaria, forårsaket av protozoan parasitt Plasmodium falciparum, overføres til mennesker ved bitt av den kvinnelige Anopheles mygg. Den sigd hemoglobin genet fører til unormale sickled røde blodceller (RBC) hos mennesker, som jf en overlevelsesfordel mot malaria i forhold til personer uten noen sigd hemoglobin gener. Som et resultat, er sigdcelleanemi utbredt i endemiske områder av malaria i Afrika og andre tropiske regioner. Detaljer om dette fenomenet er beskrevet her.
Oversikt
Malaria, forårsaket av protozoan parasitt Plasmodium falciparum, overføres til mennesker ved bitt av den kvinnelige Anopheles mygg. Den sigd hemoglobin genet fører til unormale sickled røde blodceller (RBC) hos mennesker, som jf en overlevelsesfordel mot malaria i forhold til personer uten noen sigd hemoglobin gener. Som et resultat, er sigdcelleanemi utbredt i endemiske områder av malaria i Afrika og andre tropiske regioner. Detaljer om dette fenomenet er beskrevet her.
P. falciparum
P. falciparum tar mange former og lever den seksuelle delen av sin livssyklus i mygg og aseksuell del i den menneskelige vert. I korte trekk, P. falciparum sporozoitter inn menneskeblod fra mygg spytt og reise til leveren, ta bopel og transformerer til schizonter. De schizonter reprodusere og produsere merozoites, som bryter ut fra leverceller og blir sluppet tilbake i blodet, hvor de infisere RBC. Merozoittene lever av hemoglobin og reprodusere, forming merozoites og trophozoites. Den RBC til slutt bryter ut, slippe merozoites tilbake til blodet til å infisere flere RBC, og slippe trophozoites, som forvandles til kjønnsceller. En bit av den kvinnelige Anopheles mygg plukker opp P. falciparum kjønnsceller, og parasitten reproduserer seksuelt i mygg. P. falciparum blir overført til mennesker via bitt av kvinnelige Anopheles mygg, fortsetter livssyklusen.
Forsvar
Menneskekroppen har utviklet en rekke forskjellige forsvar mot P. falciparum, hvorav den ene er den sigd hemoglobin-genet og resulterende sickled RBC-er. Den nøyaktige mekanismen som sickled RBC drepe P. falciparum er ikke fullt ut forstått, men to teorier eksisterer basert på det faktum at P. falciparum infeksjon reduserer normalt oksygennivået i sickled RBC. En hypotese er at de reduserte oksygennivåer, kombinert med sigdcelledannelse av RBCs, bevirker at sickled cellene til å bli mer unormalt formet eller sigd til enda mer, og som skal fjernes fra blodet. En annen teori er at lavt oksygennivå P. falciparum skaper i sickled RBC faktisk skader parasitten, mens dette ikke skjer i normale RBC.
Sickle Hemoglobin Genetics
En person som arver to kopier av sigd hemoglobin-gen, ett fra hver av foreldrene, utvikler sigdcelleanemi, der alle RBC har en unormal sickled form. Disse sickled RBC klumpe seg sammen og forårsake smerter, infeksjoner og organskade. I motsetning til sigdcelleanemi, er en person som arver kun en sigd hemoglobin gen sies å ha den sigdcelle egenskap og kan passere genet til avkom, men vanligvis vil ikke utvikle sigdcelleanemi. Personen vil ha færre enn sickled RBC-er sett i sigdcelleanemi, og RBC-ene som er sickled vil ikke bli sickled til graden sett i sigdcelleanemi. Sigdcelle egenskap har vanligvis ingen signifikante effekter.
Evolusjonære resultater
Selvfølgelig, den mekanismen som sickled RBC drepe P. falciparum oppstår hos personer med sigdcelle egenskap samt sigdcelleanemi. Personer med sigdcelle egenskap ikke opplever de skadelige virkningene av sigdcelleanemi, men har helt klart en overlevelse fordel fremfor individer uten sigd hemoglobin gener. Sammen med denne fordelen kommer et nødvendig onde, på grunn av genetikk. To eksemplarer av sigd hemoglobin-gen øke sjansene for å overleve malaria, men vil også føre til sigdcelleanemi, med sine skadelige og livstruende effekter. På denne måten har overlevelsen nytte av sigdcelle egenskap forårsaket sigdcelleanemi å være utbredt i områder med endemisk malaria i Afrika og andre tropiske områder.